
定了!《4+7城市药品集中采购文件》15日上午正式对外公开。
文件确定,国家组织药品集中采购试点,试点地区范围为北京、天津、上海、重庆,以及沈阳、大连、厦门、广州、深圳、成都、西安等11个城市(简称“4+7城市”)。
此次药品集中采购文件有哪些亮点?医药市场、医药企业又将如何迎战首批药品集中采购?记者集中采访药企研发、销售人员,以及药物经济学专家后,为您划出以下重点!
哪些品种入围首批采购名单?
根据已批准通过国家药品监督管理局仿制药质量和疗效一致性评价目录和按《国家食品药品监督管理总局关于发布化学药品注册分类改革工作方案的公告》〔2016年第51号〕化学药品新注册分类批准的仿制药品目录,经联采办会议通过以及咨询专家,确定31个采购品种(指定规格)及约定采购量。
31个采购品种(指定规格)及约定采购量具体如下:
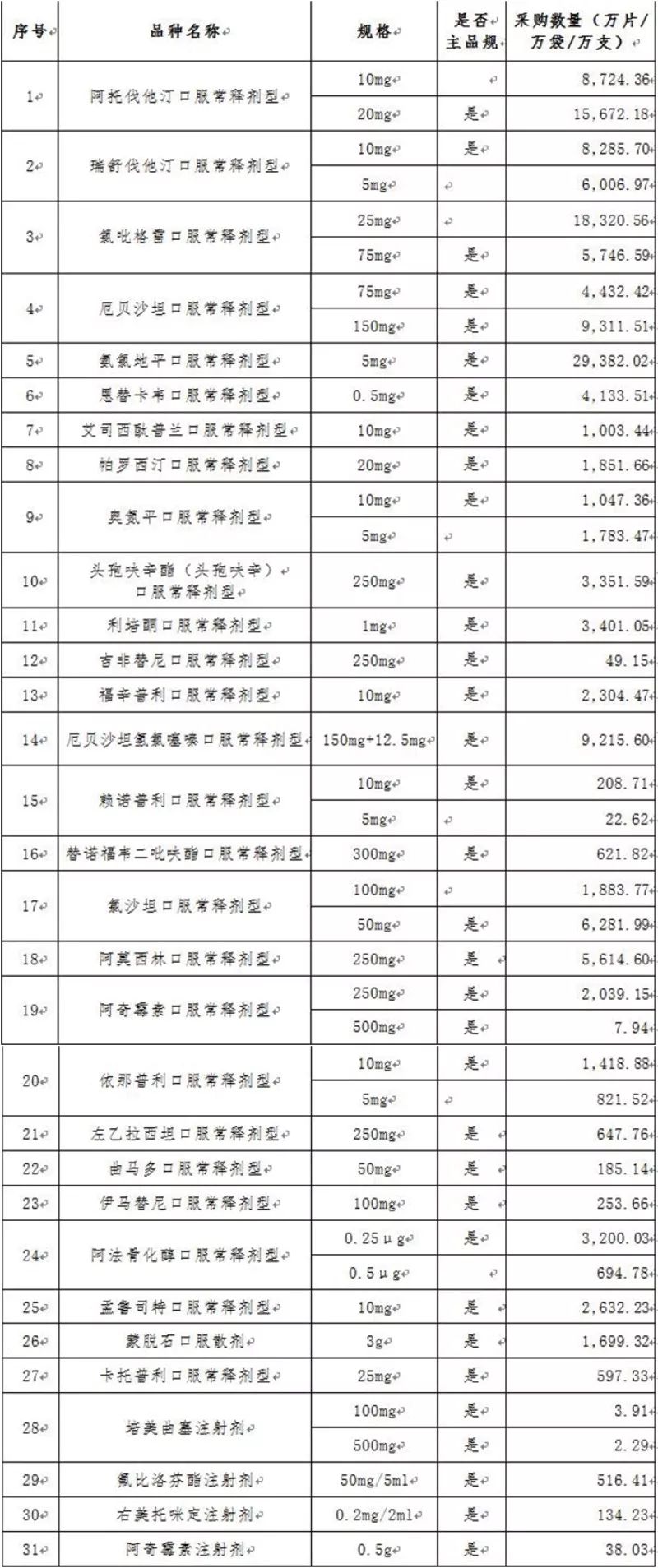
如何申报执行采购?
采购名单确定了,哪些企业具备申报资格呢?
*申报企业:
是指提供药品及伴随服务的国内药品生产企业,进口药品国内总代理商视同生产企业。
*申报要求:
1.申报企业承诺申报品种的全年产销能力达到本次采购数量要求。
2.申报品种属于采购品种目录范围,且满足以下要求之一:
2.1原研药及国家药品监督管理局发布的仿制药质量和疗效一致性评价参比制剂。
2.2通过国家药品监督管理局仿制药质量和疗效一致性评价的仿制药品。
2.3根据《国家食品药品监督管理总局关于发布化学药品注册分类改革工作方案的公告》〔2016年第51号〕,按化学药品新注册分类批准的仿制药品。
*带量采购如何执行?
各试点地区统一执行集中采购结果。集中采购结果执行周期中,医疗机构须优先使用集中采购中选品种,并确保完成约定采购量。
*采购不足怎么办?
各试点地区医疗机构在优先使用集中采购中选品种的基础上,剩余用量可按所在地区药品集中采购管理有关规定,适量采购同品种价格适宜的非中选药品。

 冀公网安备 13092302000152号
冀公网安备 13092302000152号